MINE TV
마인의 예쁨과 성형정보까지 한번에 만나보세요더많은 영상 확인하기 +
![마인 모델스토리 [남이슬님] 편](https://mineps.com/wp-content/uploads/kboard_thumbnails/5/202308/64c8aded4f5894715064-342x192.webp)
- #코성형
- #안면윤곽
마인 모델스토리 [남이슬님] 편
#성형전후 #시술 #지방흡입 #Shorts #마인성형외과 #성형외과 #추천
![마인 모델스토리 [윤소은님] 편](https://mineps.com/wp-content/uploads/kboard_thumbnails/5/202308/64c8ad59cf7545301464-342x192.webp)
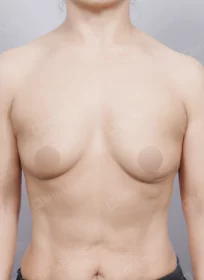
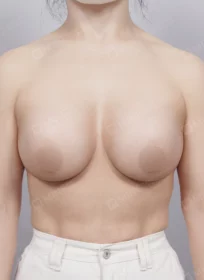
- #가슴
마인 모델스토리 [윤소은님] 편
#성형전후 #시술 #지방흡입 #Shorts #마인성형외과 #성형외과 #추천
![마인 모델스토리 <br />[근육묶기 + 지방흡입] 성형](https://mineps.com/wp-content/uploads/kboard_thumbnails/5/202308/64c8acfdd242e5361647-342x192.webp)
- #동안리프팅
- #안면윤곽
마인 모델스토리
[근육묶기 + 지방흡입] 성형
[근육묶기 + 지방흡입] 성형
#성형전후 #시술 #지방흡입 #Shorts #마인성형외과 #성형외과 #추천

- #가슴
- #체형
가슴확대를 위한
가슴보형물 수술설명
가슴보형물 수술설명
#성형전후 #시술 #지방흡입 #Shorts #마인성형외과 #성형외과 #추천

- #가슴
가슴성형에서 가장 중요한 부분은?
#성형전후 #시술 #지방흡입 #Shorts #마인성형외과 #성형외과 #추천

- #가슴
가슴성형 후 그것 언제쯤?
#성형전후 #시술 #지방흡입 #Shorts #마인성형외과 #성형외과 #추천
MINE SELFIE
예쁨의 시작
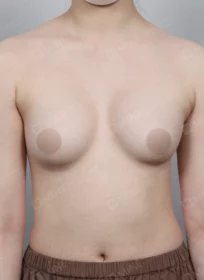
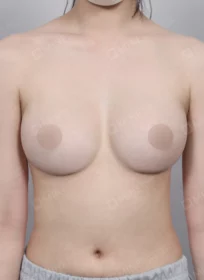
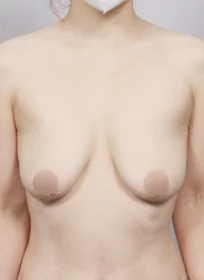
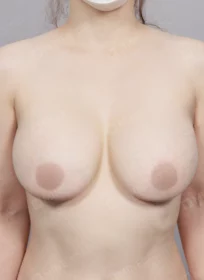
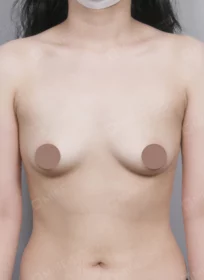
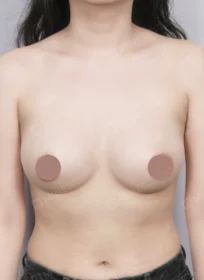
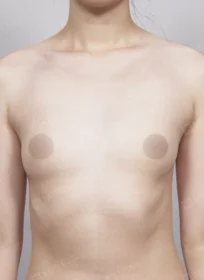
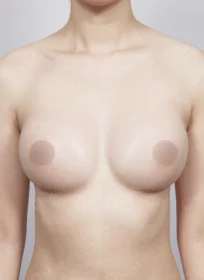
MINE BEFORE&AFTER
마인성형외과의 성형 수술 결과를 지금 바로 만나보세요
로그인 하시면 더 많은 전후사진을 볼 수 있습니다.
MINE YOUTUBE
아름다운 세상을 만듭니다.

마인티비
다양한 시술로도 해결 못하던 이중턱, 마인✨에서 해결했어요 #이중턱 #이중턱근육묶기 #shorts

마인티비
두둑한 이중턱 없애니 갸름한 브이라인이 살아났어요! #이중턱 #이중턱근육묶기 #shorts
마인티비
두툼한 턱살 이제 없어요!! 🎀 #이중턱 #이중턱근육묶기 #shorts

마인티비
이중턱 스트레스, 이제 안녕~🥰 #이중턱 #이중턱근육묶기 #shorts

마인티비
오똑하고 예쁜 코로 미모 완성✨#코성형 #코수술 #콧대 #매부리코 #성형수술 #성형외과

마인티비
이중턱만 없앴을 뿐인데, 이미지가 너무 달라졌대요😍 #이중턱 #이중턱근육묶기 #shorts

마인티비
볼록한 이중턱이요? 이제 없어요~👀 #이중턱 #이중턱근육묶기 #shorts

마인티비
흐릿하던 턱선이 이제 선명해졌어요! #이중턱 #이중턱근육묶기 #shorts

마인티비
보기싫던 이중턱 없애니까 갸름한 얼굴이 됐어요 #이중턱 #이중턱근육묶기 #shorts

마인티비
얼굴을 완성시키는 비밀, 예쁜 코✨#코성형 #코수술 #코끝 #shorts


















![[마인 Shorts] 인스타 여신이 되어 가는 중~](https://mineps.com/wp-content/uploads/kboard_thumbnails/8/202311/65681f8e237bd6643256-270x480.webp)
![[마인 Shorts] 지금 우리 병원에서 나온 얼굴?](https://mineps.com/wp-content/uploads/kboard_thumbnails/8/202311/65681c8ce4caf7735127-270x480.webp)
![[마인 Shorts] 나의 아름다움을 만드는 가장 빠른 방법은?](https://mineps.com/wp-content/uploads/kboard_thumbnails/8/202311/65681e200c97c6594589-270x480.webp)
![[마인 Shorts] 지방 흡입으로도 이렇게나 변하는 법!](https://mineps.com/wp-content/uploads/kboard_thumbnails/8/202311/6568200e4b2248869174-270x480.webp)
![[마인 Shorts] 오똑하고 예쁜 코로 미모 완성✨](https://mineps.com/wp-content/uploads/kboard_thumbnails/8/202311/65681613a40cc8127805-270x480.webp)